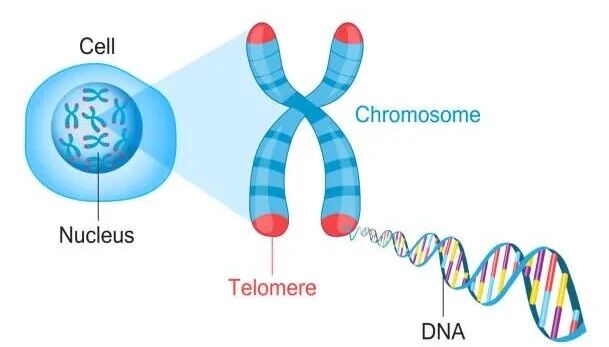
端粒DNA与一组被称为“shelterin”的保护性蛋白质紧密结合,形成一种特殊的环状结构(T-loop)。这种结构能够将染色体末端“隐藏”起来,使其不被细胞的DNA修复系统识别为断裂的DNA。如果没有这种伪装,细胞会试图“修复”正常的染色体末端,导致染色体融合或触发警报信号,迫使细胞停止分裂甚至自我毁灭。端粒存在于所有真核生物线性染色体的末端。人类拥有23对染色体,共计46条。由于每条染色体有两个末端,这意味着一个典型的体细胞中存在92个端粒——每条染色体的两端各有一个。端粒的位置并非随意。它们位于染色体末端,使其在DNA复制过程中能够充当牺牲性的缓冲区。由于DNA复制机制无法完全复制线性DNA的末端,每次细胞分裂都会丢失一小段DNA。端粒吸收了这种损失,确保编码基因的DNA尽可能长时间地保持完整。
当端粒变得过短或失去其保护结构时,细胞会以几种方式做出反应,而这些反应对健康都极为不利:
①细胞衰老:细胞进入一种永久停止分裂的状态,称为“衰老”。这些衰老细胞仍然存活,但不再参与组织生长和修复。更糟糕的是,它们会分泌炎症分子、生长因子和酶,损害周围健康组织,这种现象被称为“衰老相关分泌表型”(SASP)。随着这些“僵尸细胞”的积累,组织功能逐渐退化,促进衰老和慢性炎症。
②细胞凋亡:细胞启动程序性死亡,自我清除。虽然这有助于清除潜在的危险细胞,但大量细胞凋亡会导致组织退化和器官功能受损。③基因组不稳定:在缺乏适当保护机制的情况下,严重缩短的端粒可能导致染色体融合、断裂和突变,增加癌变风险。有趣的是,约90%的癌细胞通过重新激活端粒酶来维持端粒长度,从而绕过正常细胞的衰老机制,获得无限分裂的能力。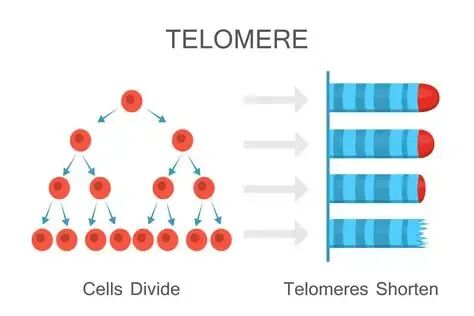
四、为什么端粒会随时间缩短
①末端复制问题:这是端粒缩短的主要原因。在DNA复制过程中,负责合成滞后链的DNA聚合酶无法完全复制染色体的3′末端。每次细胞分裂,染色体末端都会丢失一小段DNA,而端粒作为缓冲吸收了这种损失。②氧化应激:端粒DNA富含鸟嘌呤(G),这种碱基对氧化损伤特别敏感。活性氧(ROS)会直接损伤端粒DNA,或破坏保护端粒的蛋白质复合体,加速端粒损耗。吸烟、污染、炎症和不健康饮食都会增加体内的氧化负荷。③慢性炎症:持续的低度炎症会侵蚀端粒,并扰乱细胞修复机制。这种被称为“炎症衰老”的过程,是加速端粒缩短的重要因素。五、端粒在衰老过程中扮演着多大的角色
端粒被视为细胞的“生物学时钟”,其长度和缩短速度直接反映着衰老的进程,但并非衰老的唯一决定因素。研究发现,端粒长度与寿命存在显著相关性:60岁以上人群中,端粒较短者死于心脏病的风险是常人的三倍,死于传染病的风险更是高达八倍。
一是减少细胞分裂潜能,导致组织再生能力下降,表现为皮肤愈合变慢、免疫力减弱等衰老特征;二是通过衰老细胞的SASP效应,引发全身性慢性炎症,加速多器官功能退化;三是增加基因组不稳定性,提升与年龄相关疾病的发病风险。不过,端粒并非衰老的唯一驱动因素。犹他大学的研究显示,端粒长度差异仅能解释60岁以上人群死亡风险差异的4%,氧化应激、糖化反应、遗传因素等也在衰老过程中扮演重要角色。尽管如此,端粒仍是衡量“生物学年龄”的重要指标。它反映了身体所经历的累积压力——氧化应激、炎症、环境毒素,甚至心理压力都会在端粒上留下痕迹。端粒长度受遗传、环境和生活方式等多重因素共同调控,其缩短速度并非固定不变:①吸烟:每天吸一包烟持续40年,相当于额外损失7.4年的端粒寿命。 ②肥胖:肥胖女性的端粒比同龄体重正常女性显著更短,相当于衰老8.8年。 ④慢性压力:长期心理压力会增加氧化应激,加速端粒损耗。研究显示,承受高压力的女性,其端粒长度差异相当于衰老10年。 ⑤不良饮食:高加工食品、低抗氧化剂摄入加速端粒缩短。 ⑥环境污染:长期暴露于交通污染或工业化学品的人群端粒明显更短。
目前端粒长度的测量方法主要有三类,各有其适用场景和技术特点:
①Southern印迹分析,这是研究实验室的“金标准”方法。该技术能直接估算DNA千碱基中的平均端粒长度,结果准确可靠,但操作复杂、耗时费力,不适合大规模样本检测。②流式荧光原位杂交(Flow-FISH),临床诊断中的优选方法。通过荧光探针标记单个细胞内的端粒序列,能精准识别端粒极短(低于第1百分位)的患者,灵敏度达100%,特异性95%,是诊断端粒相关遗传病的关键工具。③定量聚合酶链反应(qPCR),消费级检测的常用方法。该技术快速便捷、成本较低,但与金标准的相关性中等,在区分端粒较短人群时灵敏度仅40%、特异性63%,适合提供粗略的端粒长度估计,不建议作为疾病诊断依据。
需要注意的是,端粒长度在不同组织和个体间存在差异,且会随压力、疾病和生活方式动态变化,单次检测结果难以全面反映机体的衰老状态。端粒并非“命运的决定者”。它们更像是一个生物里程表,记录着身体所经历的损耗。通过健康的生活方式——规律的体育活动、富含抗氧化剂的饮食、充足的睡眠、有效的压力管理——我们可以减缓端粒的缩短速度,支持更健康的衰老过程。虽然端粒研究仍在不断深入,但有一点已经明确:端粒是我们生活方式与衰老质量之间的一座桥梁。保护端粒,不仅是在维护遗传稳定性,更是在积极塑造未来的健康状况。正如科学家所指出的,通过消除衰老过程和修复氧化应激损伤,人类或许有潜力活得更久、更健康。而这一切,都始于对这些染色体末端“守护者”的深入了解与呵护。以上图片来自网络,本文旨在分享学习,如有侵权,请联系我们删除,谢谢!