全球首个抗衰“基因疗法”临床试验:一针逆转细胞年龄?
栏目:健康资讯 发布时间:2026-04-21
2026年3月,由哈佛大学遗传学家大卫·辛克莱(David Sinclair)联合创立的Life Biosciences公司宣布,其代号为ER-100的基因疗法,已正式完成首例受试者注射。这标志着人类历史上第一个旨在通过“细胞重编程”实现年轻化的疗法
一、ER-100是什么
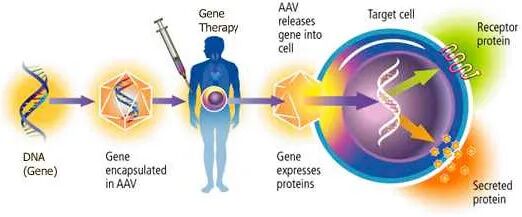
递送载体:使用一种经过改造的、无致病性的腺相关病毒(AAV),作为“运输工具”,将治疗基因安全地送入眼球内部的靶细胞。 治疗基因:三个关键的转录因子——OCT4、SOX2和KLF4,也就是著名的“山中因子”中的三个,通常被合称为OSK。 安全开关:OSK基因的表达受到一个“诱导开关”的控制,只有在个体服用特定抗生素(多西环素)时才会被激活。停药后,基因表达即关闭,这为控制重编程的“剂量”和“时间”提供了关键的安全保障。
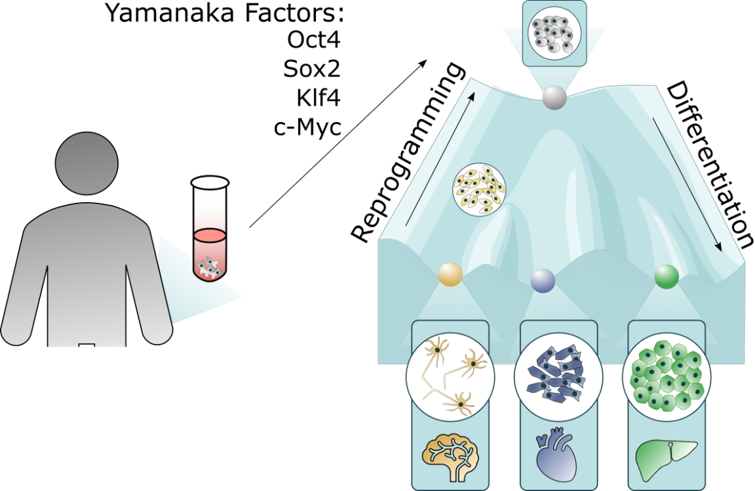
身份:属于POU转录因子家族,是维持胚胎干细胞(ESC)自我更新和多向分化潜能的核心调节因子。 功能:它是细胞重编程的“必要条件”,在自然状态下,其表达仅限于早期胚胎和生殖细胞。一旦缺失,细胞就无法被诱导回多能状态。 精妙之处:OCT4的表达水平需要被细胞精确调控,过高或过低都会导致干细胞分化或死亡。这解释了为何临床试验需要一个“开关”来精细控制其活性。
身份:属于SOX转录因子家族,通常与OCT4形成异源二聚体复合物,协同工作。 功能:它增强了OCT4与DNA结合的稳定性和特异性,共同激活下游多能性基因的表达。此外,SOX2在神经系统的发育和再生中扮演核心角色,这使得它成为干预眼科和神经退行性疾病的理想靶点。 精妙之处:单独OCT4难以发挥作用,SOX2是其最亲密、最不可或缺的合作伙伴。它们共同构成了维持细胞“干细胞特性”的分子开关。
身份:属于Krüppel样转录因子家族,具有锌指结构,功能具有高度的“上下文依赖性”。 功能:在重编程过程中,它起到“加速器”和“平衡器”的作用。一方面,它能抑制分化基因,促进细胞增殖;另一方面,它与OCT4、SOX2协同,激活多能性网络。有趣的是,它在不同环境下既可以作为癌基因,也可以作为抑癌基因。 精妙之处:它的双重身份解释了为何原始四因子中的c-Myc(一个强效癌基因)可以被它部分替代,从而降低致瘤风险。在OSK组合中,KLF4的存在是平衡重编程效率与安全性的关键。
二、“山中因子”的二十年研究历程
从“重编程”到“年轻化”的四个关键阶段
ER-100的诞生并非一蹴而就,它根植于一条清晰且坚实的科研路径。
2006年:山中伸弥团队发现OSKM四因子可将小鼠成纤维细胞重编程为iPSC。证明了分化细胞可以被“人为”逆转回多能状态,开创了细胞重编程时代。 2007年:成功诱导出人类iPSC。跨物种验证成功,为再生医学提供了潜在的自体细胞来源。 2008年:发现去除c-Myc的OSK三因子组合同样有效。首次通过“减毒”策略,规避了强癌基因c-Myc带来的风险,为临床应用铺平道路。
2012:山中伸弥与约翰·戈登共享诺贝尔生理学或医学奖,表彰“成熟细胞可重编程为多能细胞”。 2016:《Cell》发表研究,体内短暂OSKM表达可延缓小鼠衰老、改善早衰表型,首次证实重编程可对抗衰老。 2019年:研究开始聚焦于递送系统的优化(如使用非整合型病毒)。从追求“完全重编程”转向“安全、可控的部分重编程”。 2020:辛克莱团队在《Nature》封面发表重磅成果:OSK部分重编程可逆转小鼠青光眼、再生视神经、恢复视力,奠定ER-100临床前基础。

2020年(里程碑):Lu, Y.,et al. ( Nature ) 证明OSK重编程可逆转青光眼小鼠模型的视力丧失。这是ER-100最直接的临床前基础,首次在活体中证明OSK能恢复神经功能。 2024年:Browder, K.C.,et al. ( Science Translational Medicine ) 证明通过AAV靶向衰老细胞表达OSK,可改善老年小鼠多项健康指标。验证了AAV递送OSK在干预衰老相关疾病中的可行性和有效性。 2025:Life Biosciences完成IND申报全套资料,提交FDA审查。


三、获FDA批准的ER-100临床试验在做什么
开角型青光眼(OAG):一种慢性、进行性的视神经病变,是全球致盲的主要原因之一。 非动脉炎性前部缺血性视神经病变(NAION):一种因血流中断导致的“眼中风”,50岁以上人群中常见,目前无获批疗法。
给药方式:单次玻璃体内注射(直接将药物注入眼球)。 激活机制:个体在注射后需口服8周的多西环素,以“开启”OSK基因的表达。 剂量探索:先在OAG个体中测试两种不同剂量,确定安全剂量后再用于NAION个体。
安全性终点:干预后出现的不良事件(TEAEs)、剂量限制性毒性、各项实验室指标(肝肾功能、血常规等)和眼部专项检查(眼压、视力、OCT等)的变化。 长期随访:对所有参与者进行长达5年的随访,以监测任何潜在的长期副作用。
2026年1月:FDA批准IND 2026年3月:首例给药、启动招募 2026年底–2027年初:初步安全性与视力数据公布 2027年5月:主要终点完成(短期安全与耐受) 2032年3月:试验全部结束(5年长期随访)
四、对长寿医学与抗衰老行业的影响
里程碑与现实的碰撞
病因不匹配:ER-100旨在“年轻化”细胞,但青光眼的主要病因是高眼压。即使细胞变年轻了,若不解决眼压问题,疗效恐难持久。对于NAION这类“一次性”缺血事件,局部恶劣的微环境可能对新生的年轻细胞依然具有毒性。 作用机制复杂:它并非直接干预疾病,而是在存活细胞中启动一个复杂的基因表达程序,寄希望于这一系列连锁反应能最终导向功能恢复。这中间任何一个环节出错,都可能导致失败。
致癌风险:这是最大的担忧。尽管去除了c-Myc,但OSK组合本身仍具有强大的细胞重编程能力。即使在理想情况下,不形成畸胎瘤,也可能导致细胞不受控的增殖或其他不可预测的、有害的基因表达变化。著名干细胞科学家珍妮·洛林(Jeanne Loring)直言:“我担心这种疗法极有可能不安全,并导致肿瘤产生。” 免疫反应:递送基因的AAV病毒载体、来自细菌和病毒的“基因开关”组件,都可能在人体内引发意料之外的免疫反应。 脱靶效应:病毒载体可能感染非目标细胞(如视网膜的其他细胞),在这些地方激活OSK可能导致灾难性后果。


